-
Empresa
-
Nuestros productos
-
Servicios
-
Academia
Calendario científico diciembre de 2019
¿Cómo puede servir la fracción de plaquetas inmaduras (FPI) como biomarcador de episodios cardiovasculares negativos tras cirugía?
Un recuento normal de plaquetas con FPI aumentada por aumento del consumo plaquetario en sangre periférica puede ser señal de mayor agregación plaquetaria y de complicaciones tromboembólicas.
La trombocitosis con FPI reducida por una menor producción de plaquetas en la médula ósea puede ser señal de mayor agregación plaquetaria y de complicaciones tromboembólicas.
La trombocitopenia con FPI reducida por un menor consumo de plaquetas en la sangre periférica puede ser señal de mayor agregación plaquetaria y de complicaciones tromboembólicas.
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Información de base científica
La enfermedad de las arterias coronarias (EAC) es el tipo más frecuente de enfermedad cardiovascular. La EAC afecta a las arterias que llevan la sangre al corazón. La causa suele ser la aterosclerosis, por la que las arterias se estrechan ralentizando el flujo sanguíneo.
Las plaquetas no se pegan a un endotelio no activado. No obstante, procesos inflamatorios como la ateroesclerosis producen la activación del endotelio, que a su vez estimula la fijación plaquetaria. Las plaquetas desempeñan un papel esencial en la aterotrombosis en la EAC. Se consumen plaquetas en la formación de trombos, y su impacto en el recuento plaquetario se compensa con el aumento de la producción de plaquetas nuevas. Este proceso de aumento del recambio plaquetario se refleja en el aumento del recuento de plaquetas inmaduras detectadas en la sangre periférica. A menudo se ven mayores niveles de plaquetas inmaduras en circulación en pacientes con EAC, y se ha demostrado en diversos estudios que una mayor proporción de plaquetas inmaduras circulantes se relaciona con episodios cardiovasculares adversos graves (MACE) [1-3].
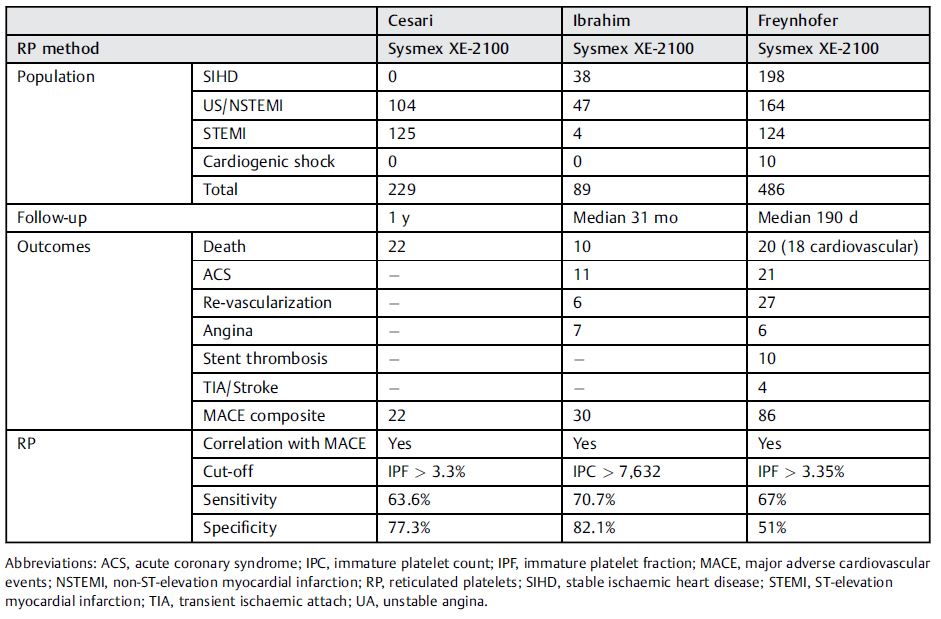
Las complicaciones tras cirugía deben identificarse en un momento temprano para posibilitar un óptimo manejo y mejorar el resultado postoperatorio. Los MACE suponen una complicación frecuente y especialmente grave, presentando una mortalidad elevada. En ese tipo de entorno, las plaquetas inmaduras han suscitado interés como factor independiente de predicción de MACE [4]. Se ha observado que la fracción de plaquetas inmaduras (FPI) es elevada en pacientes con síndrome coronario agudo [5-6], y que un recuento elevado de plaquetas inmaduras en estos pacientes se relacionaba con el aumento del riesgo de MACE después de cirugía [1]. Varios autores han descrito que existe una asociación entre una fracción de plaquetas inmaduras alta o unos valores de recuento altos por un lado, y un mayor riesgo de episodios cardiovasculares graves [1-3]. Dos de estos estudios recientes encontraron el mismo umbral de corte en 3,3 % empleando el parámetro FPI Sysmex (Tabla 1) [7].
En otro estudio reciente se evaluó si la fracción de plaquetas inmaduras (FPI) determinada en la sala de recuperación tras la anestesia podía predecir MACE u otros sucesos tromboembólicos después de cirugía no cardíaca intermedia y de alto riesgo. El primer estudio en pacientes de cirugía no cardíaca encontró que, en términos preoperatorios, no existían diferencias en la FPI entre pacientes con y sin MACE. Por otra parte, los pacientes con MACE presentaban valores en la FPI más altos en la unidad de recuperación tras la anestesia en comparación con los pacientes sin MACE. El valor del umbral óptimo de la FPI > 5,4 % se asoció a un mayor riesgo de MACE tras el ajuste de variables concomitantes [8]. Como ilustran tanto esta publicación como el caso del calendario científico este mes, la FPI es un factor de predicción independiente de MACE tras cirugía, y puede mejorar la estratificación del riesgo incluso en pacientes de cirugía no cardíaca.
Es interesante que, la reactividad de las plaquetas inmaduras medida por agregometría de transmisión de luz (ATL) no predecía MACE, y que las plaquetas inmaduras parecen actuar mejor como predictores crónicos de episodios adversos que la ATL, que es más probable que refleje el estado en el corto plazo. De forma similar, las plaquetas inmaduras son mejores a la hora de predecir MACE que la fosforilación de fosfoproteína estimulada por vasodilatadores o la agregometría de electrodos múltiples en pacientes que hayan pasado por intervenciones coronarias percutáneas [3].
Tabla
Bibliografía
[1] Ibrahim H et al. (2014) Association of immature platelets with adverse cardiovascular outcomes. J Am Coll Cardiol. Nov 18-25; 64(20):2122–9.
[2] Cesari F et al. (2013) Reticulated platelets predict cardiovascular death in acute coronary syndrome patients. Insights from the AMI-Florence 2 Study. Thromb Haemost. May; 109(5):846–53.
[3] Freynhofer MK et al. (2017) Platelet Turnover Predicts Outcome after Coronary Intervention. Thromb Haemost. May 8; 117(5):923–33.
[4] Eikelboom JW et al. (2014) Immature platelet count: part of the cardiologist's complete blood count? J Am Coll Cardiol. Nov 18-25; 64(20):2130–2.
[5] Grove EL et al. (2009) Immature platelets in patients with acute coronary syndromes. Thromb Haemost. Jan; 101(1):151–6.
[6] Lakkis N et al. (2004) Reticulated platelets in acute coronary syndrome: a marker of platelet activity. J Am Coll Cardiol. Nov 16; 44(10):2091–3.
[7] Hannawi B et al. (2018) Reticulated Platelets: Changing Focus from Basics to Outcomes. Thromb Haemost. Sep; 118(9):1517–27.
[8] Anetsberger A et al. (2017) Immature platelets as a novel biomarker for adverse cardiovascular events in patients after non-cardiac surgery. Thromb Haemost. Oct 5; 117(10):1887–95.