Calendario científico enero de 2022
Infección grave por COVID-19
¿Cuáles son los factores que han demostrado desencadenar la aparición de eritrocitos nucleados en la sangre periférica de adultos?
Anemia ferropénica
Aumento de los niveles de eritropoyetina
Niveles altos de citocinas proinflamatorias (por ejemplo, IL-6)
Hipoxemia arterial
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Fundamentación científica
Los pacientes en estado crítico debido a infecciones respiratorias pueden desarrollar síndrome de dificultad respiratoria aguda (SDRA), una enfermedad con complicaciones graves y potencialmente letal. Por lo tanto, los médicos desean contar con herramientas pronósticas fiables para prever los resultados correspondientes de forma precoz [1].
Los eritrocitos nucleados son las células progenitoras de los eritrocitos y no están presenten en la sangre periférica de los adultos sanos. No obstante, en situaciones de estrés hematopoyético, es posible detectar eritrocitos nucleados en la sangre periférica, dado que la médula ósea también secreta la estirpe de eritrocitos en fases prematuras. La presencia de eritrocitos nucleados en pacientes críticos suele relacionarse con un aumento de la mortalidad [2]. Cabe mencionar que los pacientes con presencia de eritrocitos nucleados mostraron unos niveles significativamente inferiores de presión parcial del oxígeno en la sangre arterial durante su tratamiento en cuidados intensivos respecto a los pacientes sin presencia de eritrocitos nucleados [3]. Se ha demostrado que una baja presión parcial del oxígeno en la sangre arterial apunta a la aparición próxima de eritrocitos nucleados. Asimismo, según lo observado en pacientes críticos con SDRA, parece que los eritrocitos nucleados predicen igualmente la mortalidad por SDRA [4]. Por otra parte, en los pacientes con pancreatitis aguda, los granulocitos inmaduros (GI) pueden facilitar la identificación de aquellos pacientes con alto riesgo de desarrollar SDRA [5]. Se ha considerado que los granulocitos inmaduros son un indicador potencial de la incidencia de SDRA y han demostrado una capacidad predictiva similar a otros biomarcadores (o mayor que ellos).
La reciente pandemia de SARS-CoV-2 intensificó la presión hospitalaria y en especial sobre las unidades de cuidados intensivos, que tuvieron que hacer frente con rapidez al aumento de pacientes hospitalizados por COVID-19.
Para aliviar este cuello de botella y apoyar a los hospitales en la gestión de los pacientes con COVID-19, se elaboró la puntuación pronóstica para la COVID-19 [1]. La puntuación se basa en 10 variables, disponibles de forma directa o indirecta en los analizadores de la Serie XN y ponderados con puntos en función del resultado medido (ver Tabla 1).
Las puntuaciones obtenidas durante los tres primeros días de hospitalización pueden predecir la gravedad clínica de los pacientes con COVID-19 durante las dos semanas siguientes. Se ha demostrado que la eficiencia de la puntuación supera a la de los parámetros individuales o a las proporciones de parámetros.
Tabla 1: Esquema de las variables hematológicas empleadas para la puntuación pronóstica de la COVID-19.
| Variables | |
| Variables primarias | Proporción de granulocitos inmaduros respecto a linfocitos: GI/L*100 Proporción de neutrófilos respecto a linfocitos: N/L Monocitos reactivos como porcentaje de monocitos: RE-MONO/M Linfocitos que sintetizan anticuerpos como porcentaje de linfocitos: AS-LYMPH/L Diferencia de equivalente de hemoglobina entre los reticulocitos y los eritrocitos maduros: Delta-He Eritrocitos nucleados: NRBC |
| Variables secundarias | Hemoglobina: HGB Porcentaje de células hipocrómicas: Hypo-He Recuento de plaquetas: PLT Recuento de la fracción de plaquetas inmaduras: FPI |
Resultados numéricos
Se hospitalizó a un varón de 56 años debido a síntomas intensos relacionados con la infección por COVID-19. Durante un periodo de 33 días, se observó el desarrollo de los parámetros hematológicos medidos en un analizador de la Serie XN.
En el ingreso (día 0), los resultados del hemograma completo revelaron resultados casi normales, aunque solo los valores de eritrocitos, hemoglobina y hematocrito superaban ligeramente los intervalos de referencia. El recuento diferencial automático de leucocitos mostró una distribución normal, salvo unos pocos linfocitos con un aumento de las señales de fluorescencia visibles en la parte superior del diagrama de dispersión del canal WDF.
Ya en el día 2 se observó leucocitosis (14,65 leucocitos × 10³/µL) con neutrofilia. No obstante, los neutrófilos no presentaron signos de activación (NEUT-RI 42,6 FI, NEUT-GI 153,6 SI dentro de los intervalos de referencia [6]).
El día 4, el recuento de leucocitos llegó a 17,89 × 10³/µL y el analizador indicó la presencia de GI con el mensaje «IG Present», debido a que el porcentaje de estas células aumentó al 5,1 %.
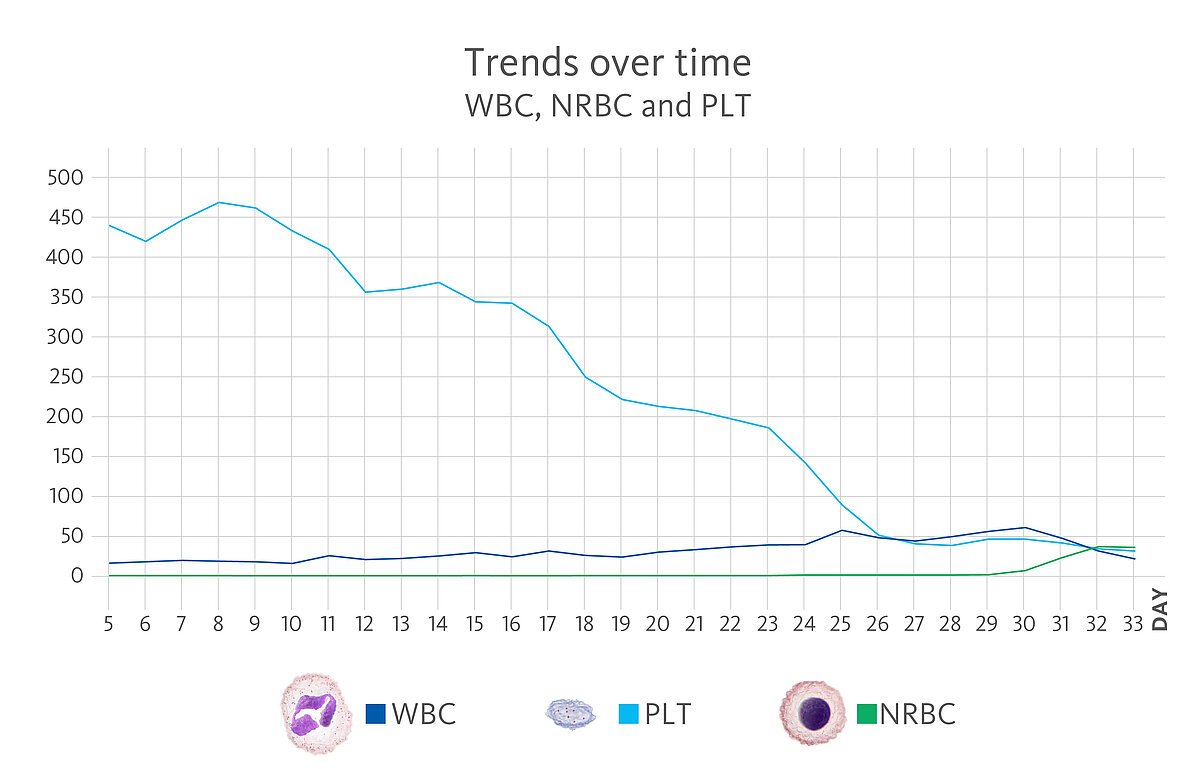
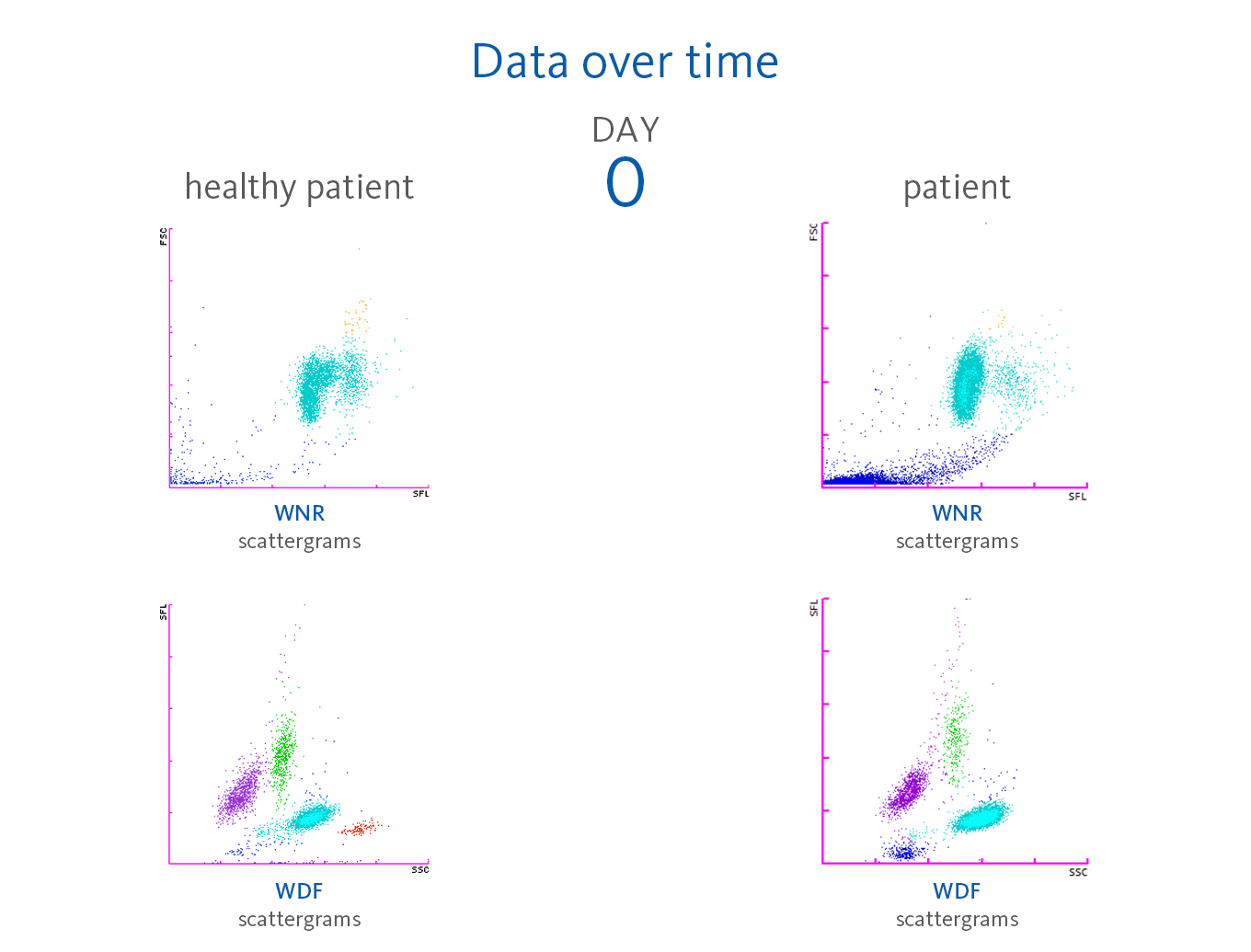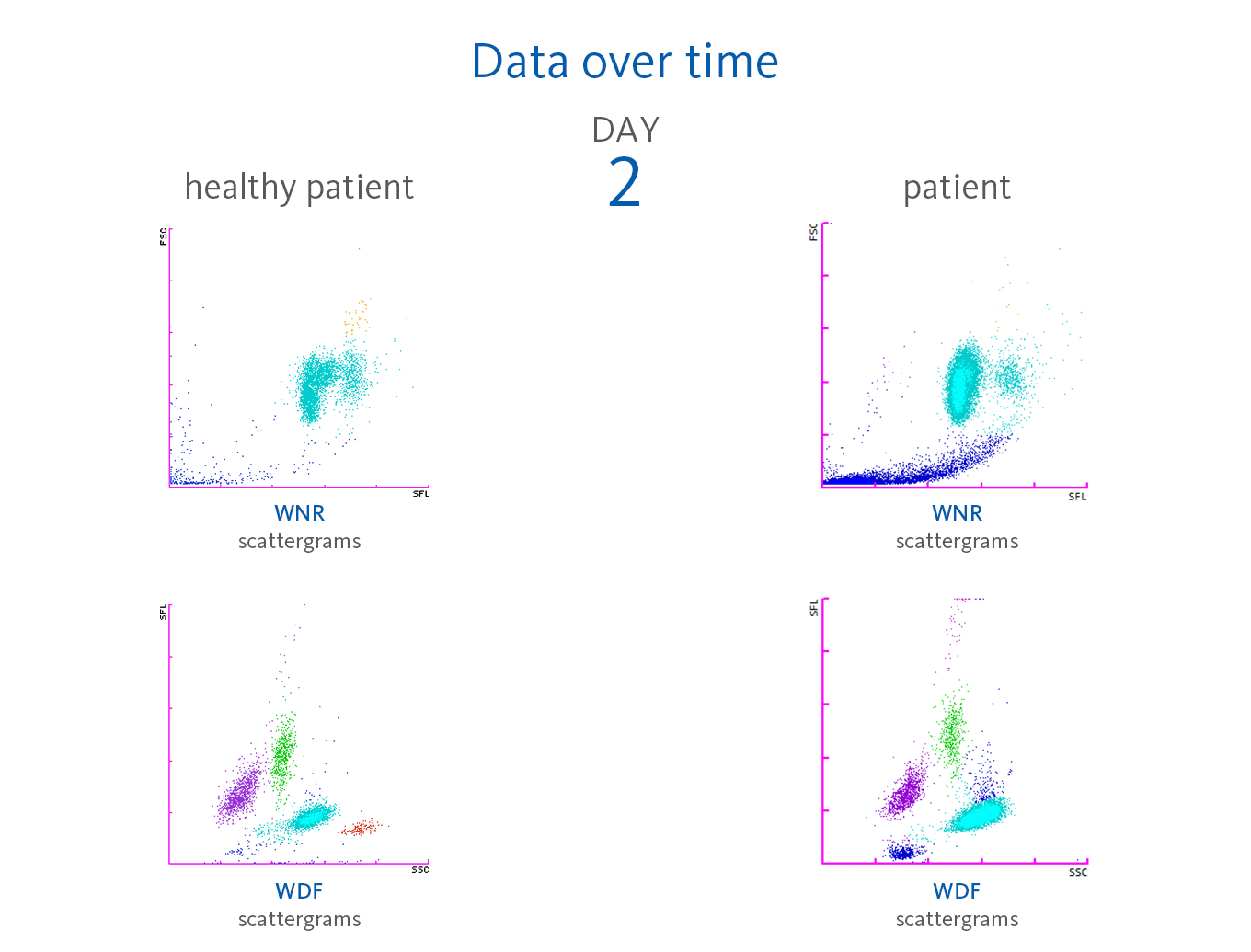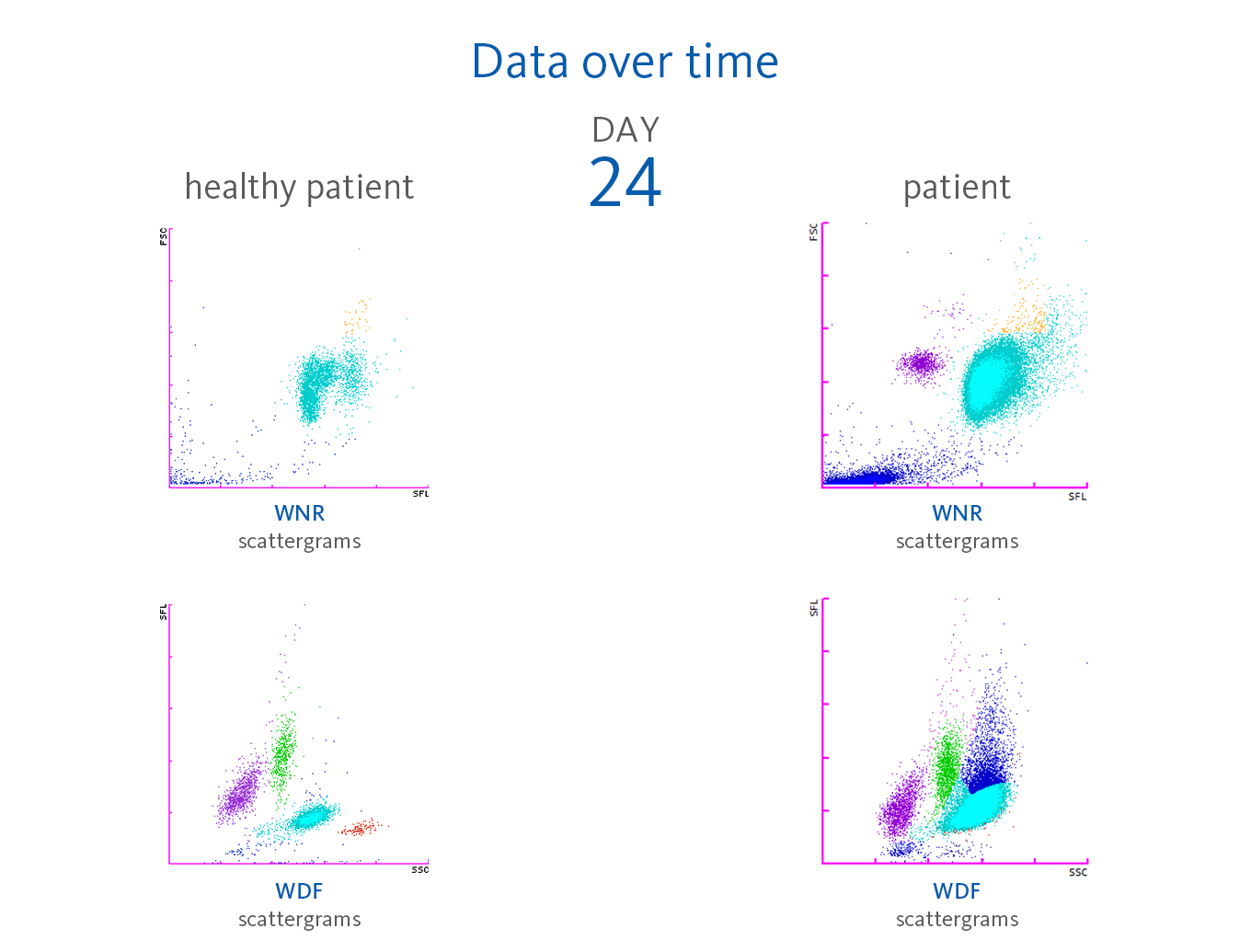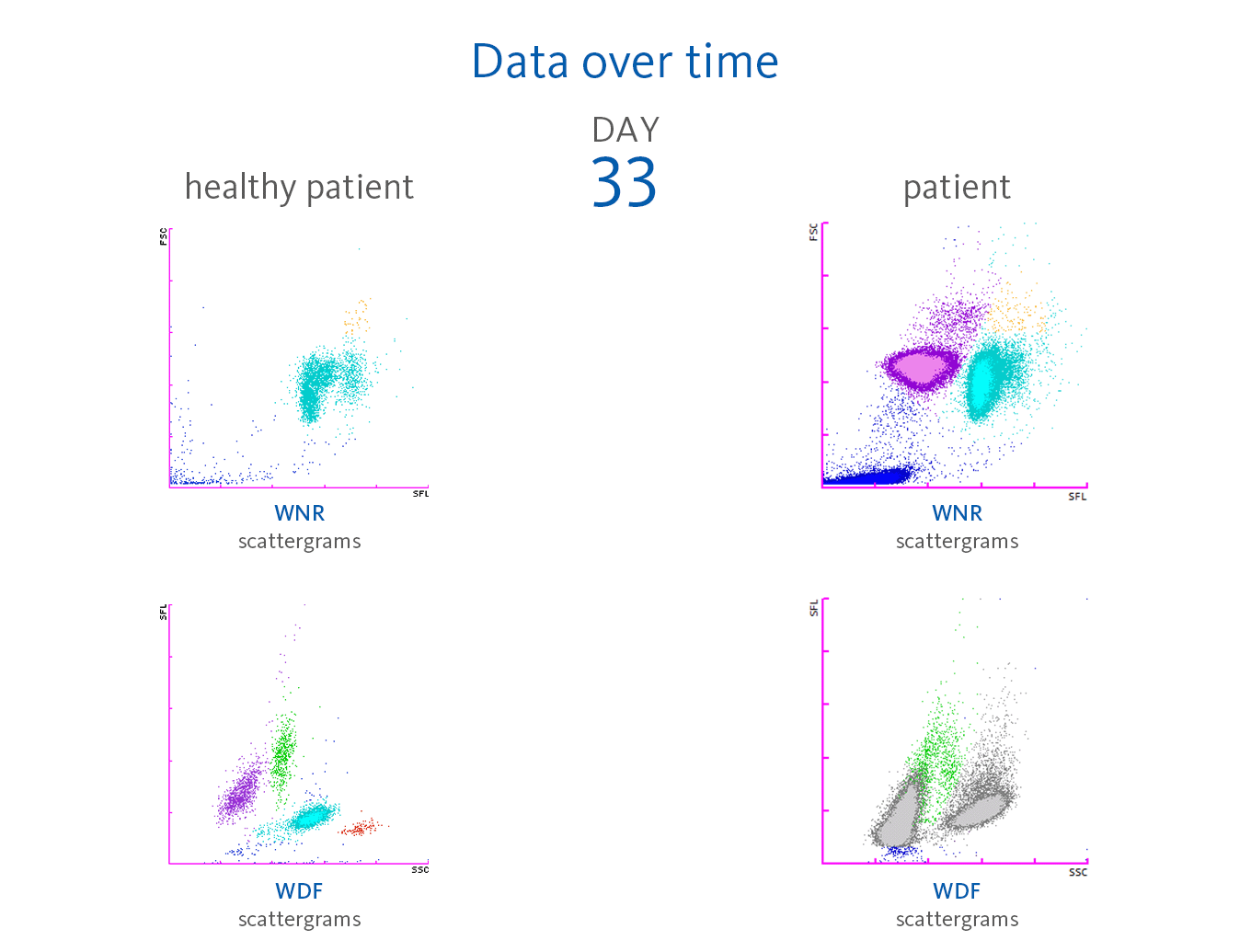
La leucocitosis evolucionó a cifras superiores con el transcurso de los días, hasta alcanzar niveles >20,00 × 10³/µL el día 11 y >30,00 × 10³/µL el día 17 con presencia de GI. Durante estas tres semanas, los eritrocitos, la hemoglobina y el hematocrito descendieron de forma continuada, mientras que las plaquetas se mantuvieron dentro del intervalo de referencia aunque ya mostraban una tendencia descendente. El día 24, se registró la primera presencia significativa de eritrocitos nucleados, con 280 células/µL (0,7 %), así como un aumento en la activación de los neutrófilos (NEUT-RI). Durante seis días consecutivos se registró la presencia de alrededor de un 2 % de eritrocitos nucleados hasta que apareció un incremento destacado:
- día 31: 11 % de eritrocitos nucleados
- día 32: 47,2 % de eritrocitos nucleados
- día 33: 116,5 % de eritrocitos nucleados
El día 26, las plaquetas descendieron por primera vez por debajo de 100 × 10³/µL, hasta alcanzar el punto más bajo el día 33 con 31 × 10³/µL. Un metaanálisis elaborado por Lippi et al. demostró que el recuento de plaquetas puede ser un parámetro de laboratorio sencillo, económico, rápido y disponible con capacidad para determinar la gravedad de los pacientes con COVID-19 de forma directa. Asimismo, se observó que la trombocitopenia también se asocia con un riesgo tres veces superior de COVID-19 grave [7].
Interpretación del diagrama de dispersión
Los analizadores de la Serie XN no solo ofrecen los recuentos absolutos y porcentuales de células, sino que también muestran los parámetros que indican activación celular. El motivo es la medición de la intensidad de fluorescencia lateral (SFL) de leucocitos en el canal WDF, lo que indica un aumento de la actividad del ARN en el citoplasma leucocitario. Los analizadores de Sysmex presentan una serie de parámetros que indican activación celular:
- Activación de los neutrófilos: intensidad de reactividad de los neutrófilos (NEUT-RI) e intensidad de granularidad de los neutrófilos (NEUT-GI)
- Activación de los linfocitos: linfocitos reactivos (RE-LYMP) y linfocitos que sintetizan anticuerpos (AS-LYMP)
- Activación de los monocitos: monocitos reactivos (RE-MONO)*
La neutrofilia estuvo presente desde el día 2. Sin embargo, no se observó una activación de neutrófilos (NEUT-RI) hasta el día 24. Ya en el momento del ingreso, se pueden reconocer linfocitos con una mayor fluorescencia en el diagrama de dispersión del canal WDF de este paciente. Gracias a las publicaciones, se sabe que en los pacientes con COVID-19 se puede observar un aumento de determinadas subpoblaciones de linfocitos a pesar de la disminución en el recuento de linfocitos. Por ejemplo, Martens et al. describen que RE-LYMP, AS-LYMP y los linfocitos de alta fluorescencia (HFLC) fueron superiores en los pacientes con COVID-19 que en el grupo de control [8].
Asimismo, cuando se hospitalizó al paciente, la población de monocitos (verde) muestra un aumento de la señal de fluorescencia visible con una tendencia al alza de la población en el diagrama de dispersión del canal WDF (ver la línea azul vertical para comparar). Se puede plantear que esta situación refleja el estado activado de los monocitos [8].
Algunos informes describen reacciones leucoeritoblásticas, definidas como la circulación de células eritroides inmaduras y células mieloides inmaduras en la sangre periférica de pacientes con infección por COVID-19 [9, 10]. En la muestra de sangre del paciente presentado, se detectó en el diagrama de dispersión del canal WNR la presencia de eritrocitos nucleados el día 24 de hospitalización y, a continuación, se observó un ascenso drástico los días 31, 32 y 33 del periodo de observación. Además, había presencia de gran cantidad de granulocitos inmaduros (mielocitos y promielocitos).
* El parámetro RE-MONO es un parámetro de servicio disponible con la versión 22.16 del software de la IPU de XN y que se puede transmitir a la IPU o el LIS Extended.
Bibliografía
[1] Linssen J et al. (2020): A novel haemocytometric COVID-19 prognostic score developed and validated in an observational multicentre European hospital-based study. Elife. 9:e63195.
[2] Stachon A et al. (2006): Poor prognosis indicated by nucleated red blood cells in peripheral blood is not associated with organ failure of the liver or kidney. Clin Chem Lab Med. 44(8):955–961.
[3] Kuert S et al. (2011): Association of nucleated red blood cells in blood and arterial oxygen partial tension. Clin Chem Lab Med. 49(2):257–263.
[4] Menk M et al. (2018): Nucleated red blood cells as predictors of mortality in patients with acute respiratory distress syndrome (ARDS): an observational study. Ann Intensive Care. 8(1):42–53.
[5] Huang Y et al. (2019): Immature granulocytes: A novel biomarker of acute respiratory distress syndrome in patients with acute pancreatitis. J Crit Care. 50:303–308.
[6] Cornet E et al. (2015): Contribution of the new XN-1000 parameters NEUT-RI and NEUT- WY for managing patients with immature granulocytes. Int J Lab Hematol. 37(5):e123–126.
[7] Lippi G et al. (2020): Thrombocytopenia is associated with severe coronavirus disease 2019 (COVID-19) infections: A meta-analysis. Clin Chim Acta. 506:145–148.
[8] Martens R et al. (2021): Hemocytometric characteristics of COVID-19 patients with and without Cytokine Storm Syndrome on the Sysmex XN-10 hematology analyzer. Clin Chem Lab Med. 59(4):783–793.
[9] Mitra A et al. (2020): Leukoerythroblastic reaction in a patient with COVID‐19 infection.
Am J Hematol. 95(8):999–1000.
[10] Milanesio M et al. (2021): Leukoerythroblastic reaction associated with COVID-19 infection. Case report. Rev Fac Cien Med Univ Nac Cordoba. 78(1):64–67. Article in Spanish.