Calendário científico agosto 2023
Monitorização precisa do tratamento de hemofilia
Que reagente TTPA não deve ser utilizado para monitorizar a terapia com Esperoct?
A escolha do reagente TTPA não é limitada de forma alguma. Qualquer reagente, seja baseado em sílica, ácido elágico ou caulino, pode ser usado para monitorizar a terapia com Esperoct.
A maioria dos reagentes TTPA baseados em sílica pode levar a uma subestimação da concentração de Esperoct infundido. Portanto, a escolha do reagente de TTPA depende do produto específico.
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Contexto
Embora a hemofilia em si seja conhecida há muitos séculos e tenha sido descrita por vários autores, a história do tratamento bem-sucedido ainda é relativamente recente. As primeiras opções de tratamento incluíam apenas o tratamento agudo de hemorragias presentes através da administração de doações de sangue total de parentes e, com a descoberta dos fatores de coagulação, a administração de transfusões de plasma. No entanto, este tipo de tratamento ainda não conseguia prevenir as hemorragias. Tal só foi possível a partir da década de 1960, quando Judith G. Pool descobriu que os crioprecipitados de plasma contêm grandes quantidades do fator VIII (FVIII). Embora esses crioprecipitados continuassem a ser usados para tratar as hemorragias nos primeiros anos, a descoberta lançou as bases para a terapia profilática, que seria alcançada pela primeira vez com o desenvolvimento de concentrados de fatores recombinantes na segunda metade da década de 1980. [1, 2]
Nos últimos anos, o desenvolvimento de preparações para a terapia de hemofilia ganhou novo impulso. Novos produtos recombinantes com semivida mais longa (SVL), baseados na modificação do fator de coagulação respetivo, modificação do fator de coagulação pela fusão da região Fc da imunoglobulina IgG1 (-Fc) ou albumina, ou a adição de polietilenoglicol (PEG) com diferentes pesos moleculares, passaram a constituir opções terapêuticas. [3] No entanto, também têm sido difundidas estratégias terapêuticas que não visam a reposição de fatores. O emicizumabe, por exemplo, é um anticorpo biespecífico monoclonal humanizado para o tratamento da hemofilia A (HA). Um lado do anticorpo liga-se ao fator de coagulação IX ativado (FIXa) e o outro ao fator de coagulação X (FX). O fármaco mimetiza, assim, a função do fator VIII ativado (FVIIIa), que está ausente ou reduzido em doentes com HA. [4] Outra opção para o tratamento de doentes com hemofilia é a terapia genética. Neste caso, uma cópia totalmente funcional do gene do fator de coagulação defeituoso na hemofilia é introduzida no corpo do doente por meio de vírus geneticamente modificados (geralmente vírus adeno-associados, VAA). A tradução do gene em células endoteliais e sinusoidais do fígado é estimulada por um promotor, de modo a que o doente possa produzir idealmente concentrações suficientes de fator de coagulação. [5]
Monitorizar o tratamento de pessoas com hemofilia de forma fiável e precisa é de grande importância para evitar hemorragias indesejadas e sequelas a longo prazo.
Ensaios de coagulação de um e dois passos, bem como ensaios cromogénicos (CSA), estão disponíveis para a determinação dos níveis de FVIII e FIX. A ocorrência de diferenças entre os resultados dos vários ensaios em hemofilia hereditária, especialmente nas formas ligeiras, é bem conhecida. [6, 7, 8, 9, 10] O mesmo se aplica aos resultados da monitorização terapêutica com concentrados de fatores de origem humana e produtos recombinantes de comprimento integral, embora os testes de coagulação de um passo e testes cromogénicos permitam essencialmente uma monitorização terapêutica precisa. Com o desenvolvimento de novos fatores de coagulação recombinantes SVL e as chamadas terapias não substitutas de fatores, surgem novos desafios para o laboratório, dada a necessidade de usar um ensaio para monitorização terapêutica em que os resultados estejam próximos do valor de tratamento calculado com base na informação do medicamento.
As discrepâncias nos resultados de diferentes testes de fator de um passo (OSA) baseados em TTPA são atribuídas a vários fatores. A escolha do reagente TTPA para determinar a atividade do fator é um desses fatores. Os reagentes TTPA diferem em termos dos fosfolípidos utilizados (de origem vegetal, animal ou recombinante) e da sua concentração, bem como da escolha do ativador. Além disso, a escolha do plasma deficiente em fatores, por exemplo, a concentração do fator von Willebrand (VWF) nos plasmas com deficiência em FVIII ou a atividade residual do plasma deficiente em fatores, também tem uma influência crítica na determinação da concentração do fator em doentes com hemofilia. Outros fatores que podem influenciar a qualidade da monitorização terapêutica de hemofilia são a escolha do calibrador (recomendando-se, em alguns casos, a utilização de calibradores específicos para o ensaio), o analisador e os protocolos de teste (análise de diluição única ou análise de diluição múltipla e linearidade do ensaio). [10, 11, 12]
Como mencionado acima, existem discrepâncias na determinação da atividade do fator entre os ensaios OSA e CSA quando determinados por estes dois métodos em doentes com hemofilia ligeira. [6, 7, 8, 9, 10] Em geral, os resultados obtidos com os ensaios OSA são mais elevados do que os obtidos pelos ensaios CSA, especialmente em doentes com HA ligeira. No entanto, o oposto (em que o resultado cromogénico corresponde à hemofilia ligeira, mas o quadro clínico não é concordante) também pode ser verdadeiro. [13]
Outro fator que não deve ser negligenciado na monitorização terapêutica da hemofilia é o próprio medicamento. Para alguns medicamentos com SVL, os ensaios OSA não são recomendados, pois subestimam a atividade do fator. Para outros medicamentos, essa limitação aplica-se apenas ao ativador usado pelo reagente TTPA. Por exemplo, ao determinar a concentração de FVIII infundido do Esperoct (N8 GP), não deve ser usada a maioria dos reagentes TTPA baseados em sílica porque a concentração de FVIII é subestimada com a utilização deste reagente, o que não acontece com outros reagentes TTPA não baseados em sílica. No entanto, é de salientar que algumas orientações específicas também excluem alguns reagentes TTPA não baseados em sílica da monitorização terapêutica do Esperoct. Para outros produtos recombinantes, a escolha do método de ensaio não é importante, pois podem ser medidos com precisão tanto por ensaios OSA quanto CSA.
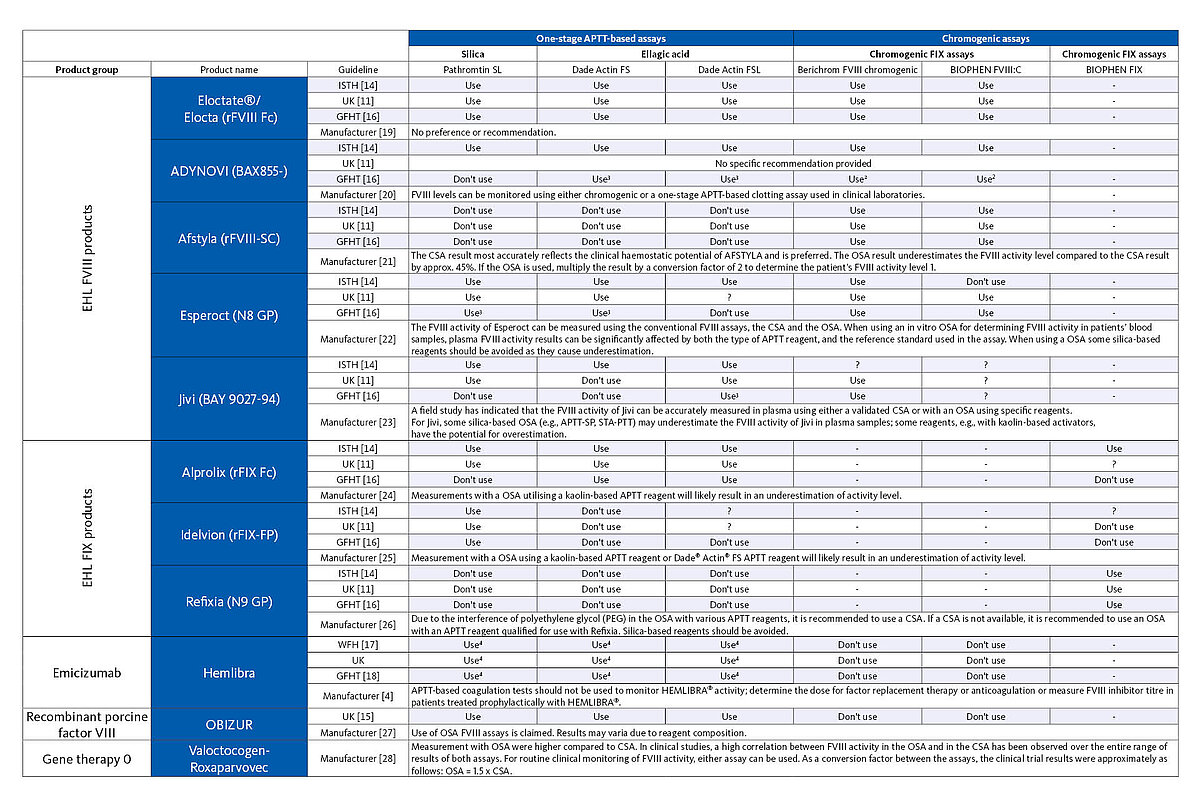
Dado o grande número de diferentes abordagens terapêuticas, é importante que o laboratório saiba qual medicamento o doente hemofílico recebeu para escolher o método de medição mais adequado para a monitorização terapêutica. A tabela abaixo apresenta uma visão geral dos sistemas de teste que devem ser usados para a monitorização terapêutica das diferentes opções de tratamento da hemofilia, de acordo com as instruções do fabricante e a opinião de especialistas.
1 Não recomendado por algumas orientações
2 Calibrador específico do produto recomendado
3 Resultados discrepantes entre estudos; a orientação recomenda o uso de ensaios cromogénicos e os resultados devem ser interpretados com cautela ou comparados com os resultados de ensaios cromogénicos se o ensaio de fator de coagulação baseado em APTT de um estágio for determinado
4 Utilização de um protocolo de ensaio modificado com maior diluição da amostra e calibrador específico de Emicizumabe
? Não especificamente suportado ou excluído
Referências
[1] Schramm W. (2014): The history of haemophilia - a short review. Thromb Res. 2014 Nov;134 Suppl 1: S4-9.
[2] Franchini M, Mannucci PM. (2014): The history of hemophilia. Semin Thromb Hemost. 2014 Jul;40(5):571-6.
[3] Young G, Mahlangu JN. (2016): Extended half-life clotting factor concentrates: results from published clinical trials. 2016 Jul;22 Suppl 5:25-30.
[4] Hemlibra® (2022): Leitfaden für medizinisches Fachpersonal, Version 3.0, Stand: Dezember 2022. Roche Pharma AG.
[5] ROCTAVIAN (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[6] Bowyer AE, Van Veen JJ, Goodeve AC, Kitchen S, MakrisM. (2013): Specific and global coagulation assays in the diagnosis of discrepant mild hemophilia A. Haematologica 2013;98(12):1980–1987
[7] Baig MA, Swamy KB. (2021): Comparative analysis of chromogenic vs clot-based one stage APTT assay for determination of factor VIII level. Indian J Pathol Microbiol. 2021 Jan-Mar;64(1):123-127.
[8] Potgieter, J.J., Damgaard, M. and Hillarp, A. (2015): One-stage vs. chromogenic assays in haemophilia A. Eur J Haematol, 94: 38-44.
[9] Annette E. Bowyer, Robert C. Gosselin. (2022): Factor VIII and Factor IX Activity Measurements for Hemophilia Diagnosis and Related Treatments. Semin Thromb Hemost, available online at DOI: 10.1055/s-0042-1758870.
[10] Pouplard C, Trossaert M, Le Querrec A, et al. (2009): Influence of source of phospholipids for APTT- based factor IX assays and potential consequences for the diagnosis of mild haemophilia B. Haemophilia. 2009;15(1):365-368.
[11] Gray E, Kitchen S, Bowyer A, et al. (2020): Laboratory measurement of factor replacement therapies in the treatment of congenital haemophilia: A United Kingdom Haemophilia Centre Doctors’ Organisation guideline. Haemophilia. 2020; 26:6–16.
[12] Nougier C, Sobas F, Nguyen TK, et al. (2011): Analytic variability due to change of deficient plasma vials: application to one-stage clotting factor VIII assay. Blood Coagul Fibrinolysis 2011;22: 151–154.
[13] Bowyer AE, Goodeve A, Liesner R,Mumford AD, Kitchen S, Makris M. (2011): p.Tyr365Cys change in factor VIII: haemophilia A, but not as we know it. Br J Haematol 2011;154(5):618–625.
[14] Peyvandi F, et al. (2020): Laboratory testing in hemophilia: Impact of factor and non-factor replacement therapy on coagulation assays. J Thromb Haemost.; 18: 1242–1255.
[15] Bowyer A, Gray E, Lowe A, et al. (2022): Laboratory coagulation tests and recombinant porcine factor VIII: A United Kingdom Haemophilia Centre Doctors’ Organisation guideline. Haemophilia. 2022;1-5.
[16] Jeanpierre E, Pouplard C, Lasne D, et al; On behalf of the French Study Group on the Biology of Hemorrhagic Diseases (the BIMHO group). (2020): Factor VIII and IX assays for post-infusion monitoring in hemophilia patients: Guidelines from the French BIMHO group (GFHT). Eur J Haematol. 2020; 105:103–115.
[17] Srivastava A, et al. (2020): WFH Guidelines for the Management of Hemophilia, 3rd edition. Haemophilia: 26 (Suppl 6): 1 – 158.
[18] Nougier C, et al. (2020): Emicizumab treatment: Impact on coagulation tests and biological monitoring of haemostasis according to clinical situations (BIMHO group proposals). Eur J Haematol.; 105: 675–681.
[19] Elocta (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[20] ADYNOVI (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[21] AFSTYLA (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[22] Esperoct (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[23] Jivi (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[24] Alprolix (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[25] Idelvion (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[26] Refixia (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[27] OBIZUR (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.
[28] Valoctocogen-Roxaparvovec (2023): SUMMARY OF PRODUCT CHARACTERISTICS. Retrieved from EMA, 26 June 2023.