Calendário científico junho 2020
Nefropatia hipertensiva
Porque é que a utilização de Sysmex Meditape 11A no UC-3500 é uma ferramenta ideal no rastreio da albuminúria?
Devido ao seu limite de deteção de 5,5 mg/l
Porque também inclui a taxa de filtração glomerular
Porque fornece uma avaliação correta por correlação com a creatinina
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Informação científica de suporte
A doença renal crónica (DRC) é definida como uma anomalia na estrutura ou na função renal presente durante mais de três meses. A classificação da DRC baseia-se na taxa de filtração glomerular (eGFR) e na albuminúria [KDIGO]. A DRC faz parte de um contínuo patológico com vários fatores responsáveis pela promoção da progressão de doença renal aguda (DRA) para doença renal crónica e, posteriormente, para falência renal (end-stage renal disease, ESRD).
Para além de uma série de patologias diferentes, tais como obstruções renais persistentes, infeções crónicas do trato urinário inferior, nefrite intersticial e doença renal poliquística, a hipertensão é a segunda causa principal de falência renal, a seguir à diabetes mellitus.
A hipertensão pode ser quer uma causa, quer uma consequência da doença renal crónica e contribui para a sua progressão, uma vez que afeta todos os compartimentos renais: vasos sanguíneos, glomérulos e espaço tubular intersticial.
A hipertensão crónica provoca nefropatia hipertensiva que se manifesta como nefroesclerose hipertensiva através da deposição de hialina (hialinose) nas arteríolas aferentes, conduzindo a alterações mínimas na hemodinâmica intraglomerular. Contudo, uma hialinose contínua provoca um estreitamento e alterações estruturais da aorta e artérias, reduzindo a sua elasticidade e a hemodinâmica. Estas alterações estruturais e o stress mecânico relacionado traduzem-se em lesões glomerulares (glomerulopatia hipertensiva), por exemplo, por isquemia parcial, estreitamento do lúmen glomerular e redução da taxa de filtração glomerular. Nos glomérulos, os podócitos interagem formando uma barreira de filtração seletiva por tamanho, essencial para a filtração glomerular e produção de urina. A hipertensão provoca lesões nos podócitos que se desligam irreversivelmente da membrana glomerular basal, danificando a barreira, o que conduz a proteinúria. A hipertensão provoca ainda um vasto espetro de lesões nas células epiteliais tubulares renais (CETR), conduzindo posteriormente a uma perda celular e à libertação de substâncias pró-inflamatórias. A angiotensina II, um agente vasoconstritor do sistema renina-angiotensina que regula a pressão arterial, é um promotor conhecido da inflamação e stress oxidativo através da indução de citocinas e quimiocinas. Esta interação induz a transformação de células epiteliais em células mesenquimatosas através da perda da polaridade celular e alteração da adesão celular, conduzindo a fibrose tubulointersticial e progressão da doença renal crónica [SECCIA].
Resultados laboratoriais
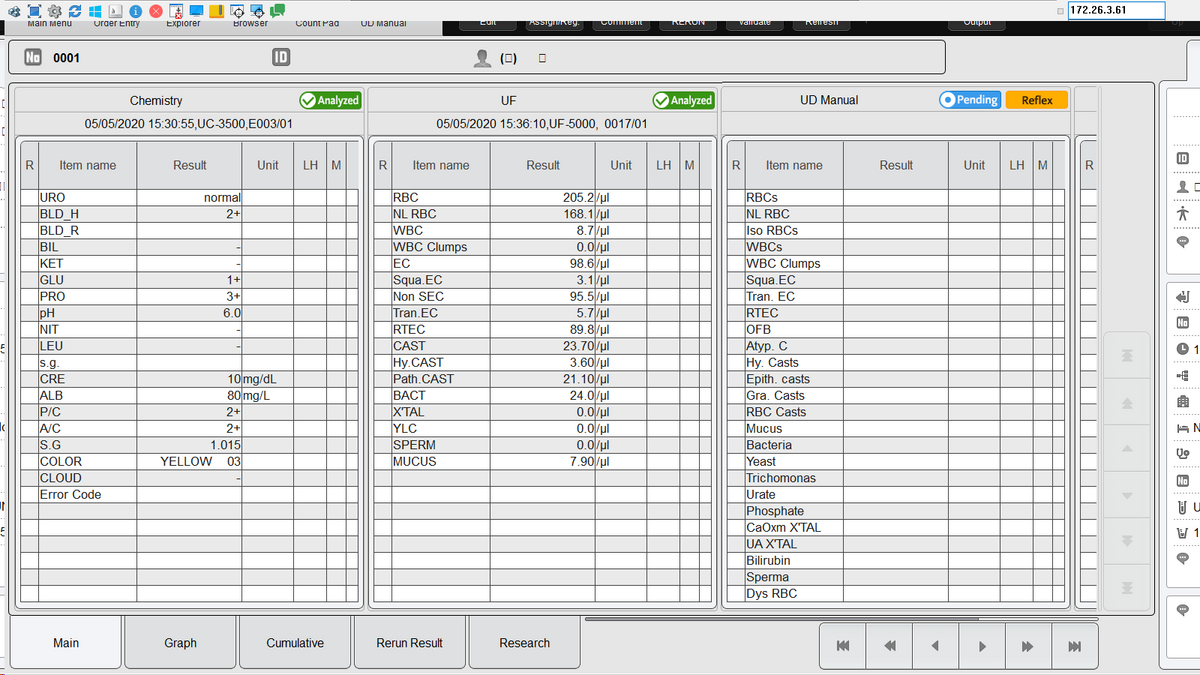
1. Apresentação do resultado da análise de urina no U-WAM
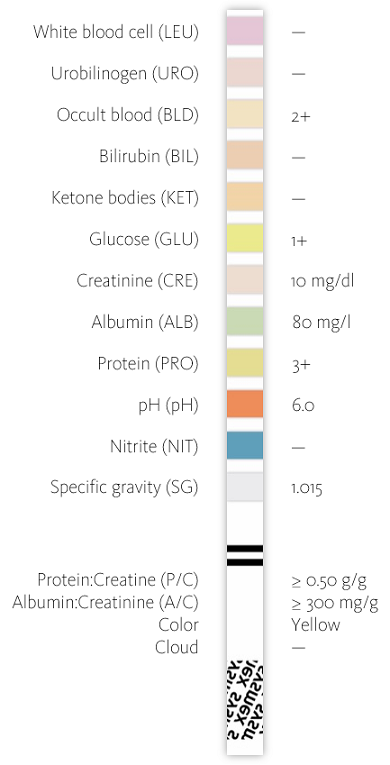
2. Teste em tiras no UC-3500
O teste em tiras revelou uma proteinúria acentuada com uma albuminúria moderadamente aumentada (anteriormente designada de “microalbuminúria”). Dado que a presença de proteínas na urina e concentração de albumina podem ser afetadas por sudação intensa ou ingestão de líquidos, a correlação com o valor da creatinina é um procedimento usual para obter uma informação para diagnóstico exata. Neste caso, quer a razão proteína:creatinina quer a razão albumina:creatinina confirmaram albuminúria e proteinúria severamente aumentadas.
A utilização das tiras de teste Meditape 11A no UC-3500 com a sua tecnologia de sensor CMOS demonstram o potencial de deteção e quantificação altamente sensíveis da albuminúria num campo de teste baseado na ligação a um corante. As concentrações de albumina podem não só ser classificadas, mas também quantificadas com um limite de deteção de 5,5 mg/l. Tal permite não apenas a determinação da albuminúria em intervalos de albuminúria moderadamente elevada, mas também em intervalos fisiológicos, comparável com a análise imunonefelométrica [DELANGHE].
3. Células epiteliais tubulares renais (CETR) no UF-5000
O UF-5000 detetou as células epiteliais tubulares renais (CETR). As CETR cobrem os túbulos renais desde o túbulo proximal, ao longo da ansa de Henle, até ao túbulo distal, e desempenham um papel vital na regeneração renal, embora também libertem moléculas pró-inflamatórias responsáveis pela progressão da doença renal crónica. Apesar de a urina de pessoas saudáveis poder conter algumas CETR devido à exfoliação normal, a presença de ≥ 15 CTER (por 10 HPFs) indica a presença de doença renal ativa ou lesão tubular.
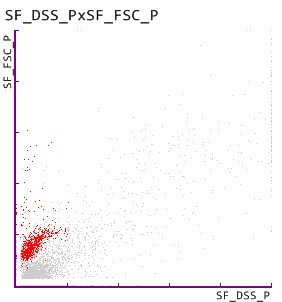
4. Eritrócitos dismórficos no UF-5000
O UF-5000 confirma ainda a hematúria indicada pelo UC-3500 através da deteção de eritrócitos dismórficos, que são um indicador conhecido de lesão glomerular [Fairly and Birch].
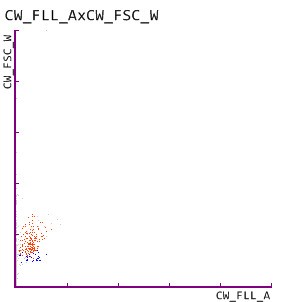
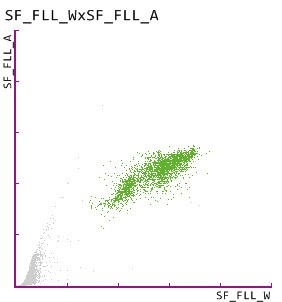
5. Cilindros urinários no UF-5000 e UD-10
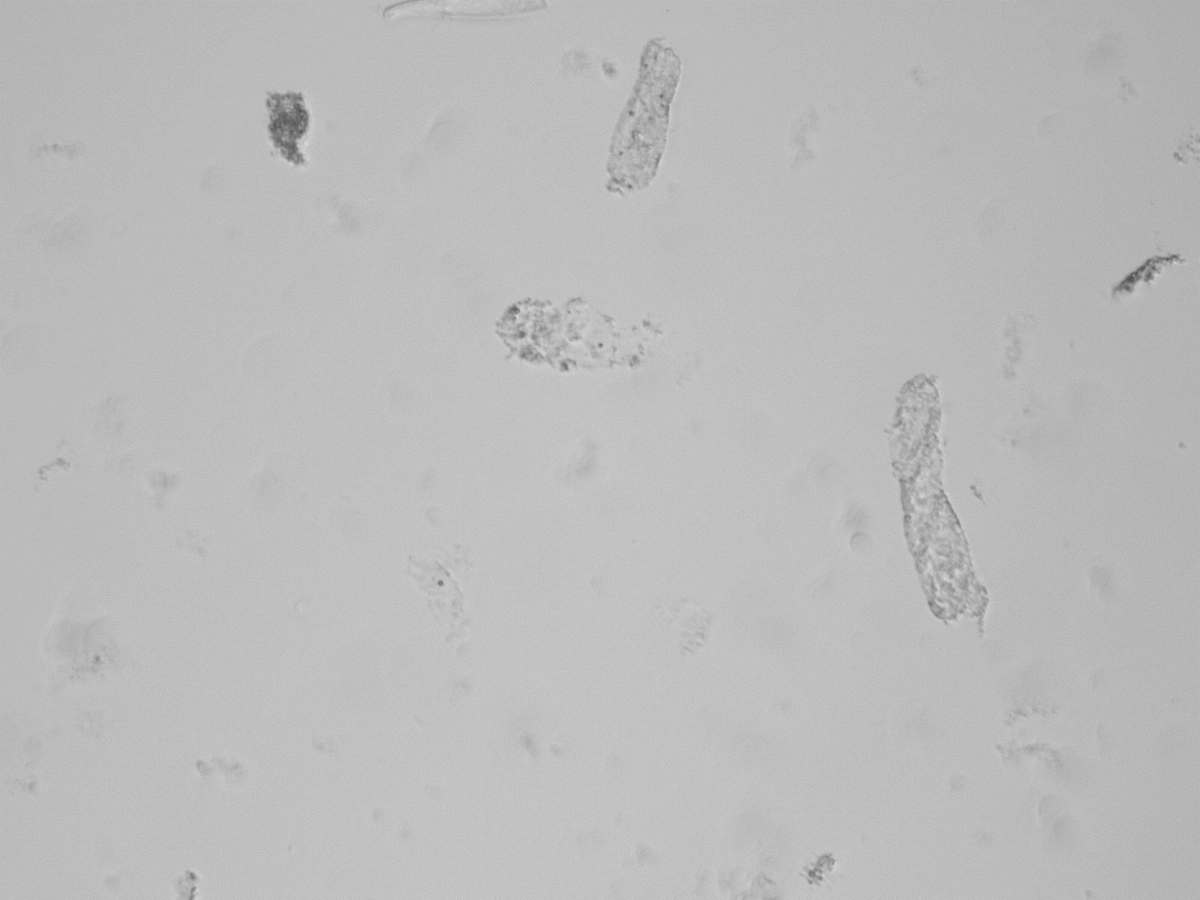
6. Imagens dos cilindros patológicos obtidas com o UD-10
A glicoproteína uromodulina, também conhecida como proteína de Tamm-Horsfall, é sintetizada exclusivamente pelas células tubulares renais da região distal da ansa de Henle [BACHMANN]. A precipitação e agregação da uromodulina nos túbulos renais conduz à formação de cilindros urinários. Os cilindros hialinos são frequentemente observados em indivíduos saudáveis, mas a sua quantidade aumenta em caso de doença renal em curso. Os cilindros patológicos, tais como os indicados no diagrama de dispersão acima, apontam para uma doença renal e a sua presença foi confirmada por deteção de cilindros patológicos no UD-10.
Referências
Bachmann S, Koeppen-Hagemann I, Kriz W (1985): Ultrastructural localization of Tamm-Horsefall glycoprotein (THP) in rat kidney as revealed by protein A-gold immunocytochemistry. Histochemistry 83(6):531–538.
Cassia MA, Pozzi FE, Bascapè S, Saggiante L, Daminelli G, Cirelli C, Damavandi PT, Elli M, Gallieni M (2016): Proteinuria and albuminuria at point of care. Point of Care 2(1):e8–e16.
Delanghe JR, Himpe J, De Cock N, Delanghe S, De Herde K, Stove V, Speeckaert MM (2017): Sensitive albuminuria analysis using dye-binding based test strip. Clin Chim Acta 471:107–112.
Enko D, Stelzer I, Boeckl M, Derler B, Schnedl WJ, Anderssohn P, Meinitzer A and Herrmann M (2020): Comparison of the diagnostic performance of two automated urine sediment analysers with manual phase-contrast microscopy. Clin Chem Lab Med 58(2):268–273.
Fairley JK, Owen JE, Birch DF (1983): Protein composition of urinary casts from healthy subjects and patients with glomerulonephritis. Br Med J 287(6408):1838–1840.
KDIGO (2012): Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013; 3:1–150.
Oyaert M, Delanghe JR (2019): Semiquantitative, Fully Automated Urine Test Strip Analysis. J Clin Lab Anal 33(5):e22870.
Pugh D, Gallacher PJ, Dhaun N (2019): Management of Hypertension in Chronic Kidney Disease. Drugs 79:365–379.
Seccia TM, Caroccia B, Calo LA (2017): Hypertensive nephropathy. Moving from classic to emerging pathogenetic mechanisms. Journal of Hypertension 35:205–212.